油价回落催化风险偏好修复,欧洲股指期货集体反弹
汇通财经APP讯——根据 汇通财经APP 报道,欧洲股市期货集体反弹,欧洲斯托克50指数期货上涨1.4%,德国DAX指数期货上涨1.2%,英国富时100指数期货上涨0.59%。这一走势反映市场情绪快速修复,风险偏好回升,成长型与出口导向板块领涨。
本次欧洲股指期货反弹主要由多重利好共振驱动:
1.地缘风险边际缓和(最直接触发)
特朗普近期表态“对伊朗战事将很快结束”,缓解市场对中东冲突升级的担忧。国际油价(布伦特原油)从高位回落超10%(最新报价约91-94美元/桶区间),全球避险情绪降温。此前因油价暴涨引发的恐慌抛售转为逢低买入,欧洲高Beta市场弹性放大。
2.能源成本压力缓解利好出口型经济
德国等制造业大国高度依赖能源进口,油价与天然气回落直接降低企业生产成本,提升盈利预期。DAX成分股中汽车、化工、工业设备等出口企业受益突出,期货反弹斜率领先。
3.英国富时100防御属性凸显
富时100成分股中能源、金融、消费必需品权重较高,油价回落虽对能源股构成一定利空,但同时缓解通胀压力,有助于英国央行更早宽松路径,支撑银行与公用事业股估值修复。涨幅相对温和体现其防御特性。
4.技术性修复与资金回补
前期地缘紧张导致欧洲股指超跌,估值压缩至低位。风险偏好转向触发空头回补与抄底资金流入,斯托克50作为泛欧洲成长股代表,弹性最强,涨幅居前。
以下表格对比三条主要指数期货表现及关键特征(基于最新市场数据):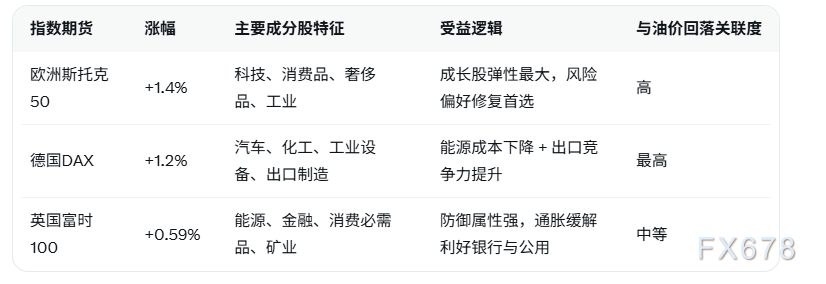
短期来看,反弹行情仍有延续空间,但波动性仍较高。地缘局势虽边际改善但不确定性犹存,油价、通胀及全球央行路径可能反复扰动。欧洲股市对外围敏感,易出现脉冲拉升后震荡。资金“低位回补”逻辑支撑底部,但需警惕获利了结压力。
中期视角偏积极,欧洲核心资产修复动能充足。欧元区制造业PMI若企稳回升、能源成本持续低位,将强化企业盈利预期。欧洲央行降息周期加速预期也将支撑估值修复。重点跟踪:① 油价企稳信号;② 欧元区PMI与工业产出数据;③ 欧洲央行3月议息会议前瞻指引。
风险提示 1.地缘冲突超预期升级导致油价反弹、流动性收紧 2.全球经济数据偏弱,出口与消费双双不及预期 3.美联储路径扰动引发美元强势与风险偏好回落
编辑总结
欧洲股指期货集体反弹,斯托克50领涨1.4%,DAX涨1.2%,富时100涨0.59%,核心驱动为中东地缘风险缓和与油价大幅回落。前期超跌估值优势得到验证,中长期看能源成本下降与货币政策宽松预期将支撑修复行情,但外部不确定性仍需警惕阶段性调整。
【常见问题解答】
1.问:本次欧洲股指期货反弹的最主要触发因素是什么?
答:最直接触发是地缘风险缓和。特朗普表态“对伊朗战事将很快结束”迅速缓解市场对中东冲突长期化的担忧,国际油价从高位回落超10%,全球风险偏好修复。此前因能源价格暴涨引发的避险抛售转为逢低买入,欧洲作为高Beta市场弹性最大,斯托克50与DAX涨幅领跑。
2.问:为什么德国DAX反弹幅度明显强于富时100?
答:DAX成分股以出口导向型制造业为主(如汽车、化工、工业设备),油价与天然气价格回落直接降低生产成本,提升盈利预期与出口竞争力。富时100则以能源、金融、消费必需品权重较高,油价下跌对能源股构成利空,防御属性更强导致涨幅相对温和。
3.问:当前欧洲股指估值是否具备吸引力?
答:前期暴跌后估值已显著压缩,斯托克50与DAX当前PE处于历史相对低位区间。前期回调幅度大,叠加油价稳定预期与欧洲央行宽松路径,修复空间较大,性价比突出。
4.问:后市短期波动加大的主要风险点有哪些?
答:地缘局势不确定性犹存,可能导致油价反复;外资或获利了结压力;美联储路径若偏鹰派,美元强势将压制风险资产。波动放大,但底部资金回补逻辑提供支撑。
5.问:投资者如何把握本次反弹的配置机会?
答:短期接受震荡,优先左侧布局成长与出口核心资产(如斯托克50成分股中的科技、奢侈品、工业龙头,或DAX中的汽车与化工股),可通过相关ETF分散风险。动态关注油价企稳、欧元区PMI及欧洲央行指引,作为加仓或减仓信号。整体控制仓位,捕捉中期估值修复与盈利改善机会。


