石藥集團(01093.HK)SYHX2011G1在美國獲臨床試驗批准
相關文章
- 36分鐘前
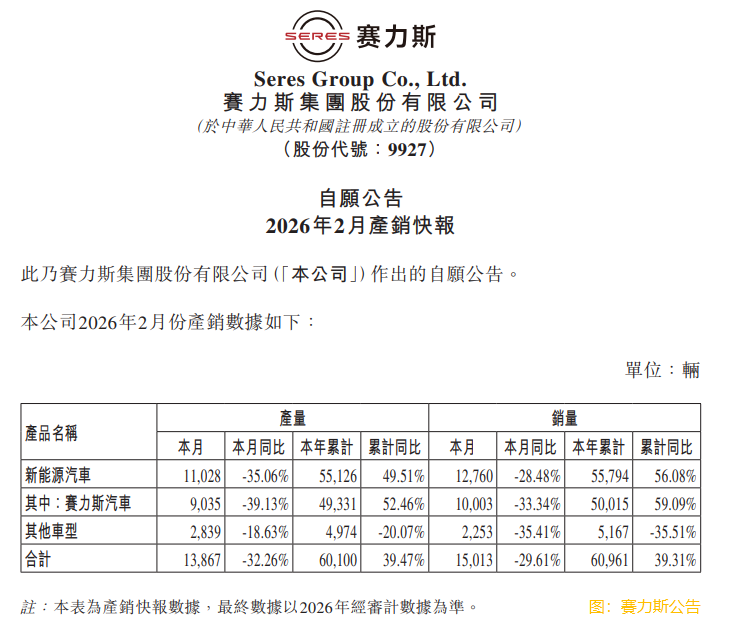
- 賽力斯(09927.HK)2月汽車銷量合計15013輛
- 1小時前
- 塗鴉智能-W(02391.HK)涨超4% 2025年淨利潤5789萬美元 同比增逾10倍
- 1小時前
- 華領醫藥-B(02552.HK)多格列艾汀在中國香港獲批上市
- 2小時前
- 愛康醫療(01789.HK)獲納入中證港股通機器人主題指數成份股
- 17小時前
- 太平洋網絡(00543.HK)料年度股權持有人應佔淨虧損500萬元至盈利500萬元
- 17小時前
- 蜆壳電業(02381.HK)料年度公司擁有人應佔溢利應800萬至1200萬港元
- 17小時前
- 【盈警】榮陽實業(02078.HK)料2025年盈轉虧至5921萬港元
- 18小時前
- 潼關黃金(00340.HK)獲納入富時全球股票指數系列
- 20小時前
- 創聯控股(02371.HK)訂立第三份補充協議以進一步延長最後完成日期至3月31日
- 20小時前
- 中國供應鏈產業(03708.HK)股份簡稱3月5日起改為「世界數字經濟產業」